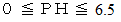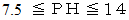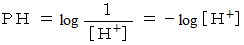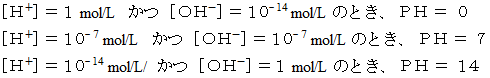酸化還元反応 と 酸塩基反応
 生理学 へ戻る
生理学 へ戻る
 人間の体のしくみ へ戻る
人間の体のしくみ へ戻る
2012.08.03_______
(1) 酸化還元反応
還元剤 から 酸化剤 に 電子 を渡す反応のこと。
酸化還元反応により、 還元剤は酸化され、 酸化剤は還元される。
「 還元剤 電子を渡して 酸化され 」
「 酸化剤 電子を受け取り 還元され 」
酸化 : 酸素原子を得ること、 または、 水素原子を失うこと、 または、 電子を失うこと。
還元 : 酸素原子を失うこと、 または、 水素原子を得ること、 または、 電子を得ること。
( 例 )
2H2 + О2 → 2H20
水素の燃焼は、2個の還元剤としての水素が電子を 1 個ずつ
酸化剤としての酸素に授受する。
Cu0 + H2 → Cu + H20
2 H2S + 02 → 2S + 2H20
(2) 酸塩基反応
酸 から 塩基 に 水素イオン を渡す反応のこと。
酸塩基反応によって、 酸 も 塩基 も中和され、 塩 ができる。
たとえば、 酸としての塩酸が 1 個の水素イオンを塩基としての水酸化ナトリウム
に渡して、 水 と 塩としての塩化ナトリウム ができる。
「 水素イオン 渡した酸は 中和され 」
(3) 酸性・アルカリ性
酸性: 一般的には 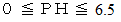
中性: 一般的には 
アルカリ性: 一般的には 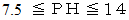
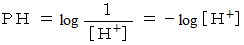
※ ただし log は 常用対数( 底が10の対数 )
水素イオン濃度が高いほどPHは低い。
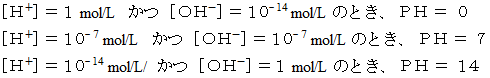
 生理学 へ戻る
生理学 へ戻る 人間の体のしくみ へ戻る
人間の体のしくみ へ戻る